纳米技术加速生物医学创新,NanoCoulter助力外泌体研究再突破!
在纳米技术与生物医学的交汇点,一场关于诊断、治疗和精准药物递送的革新正加速上演。近年来,外泌体——这一细胞间信息传递的“信使”——吸引了科研界的广泛关注。它们不仅承载着丰富的生物信息,参与细胞间的物质交换,还展现出巨大的临床应用潜力。
然而,如何精准分析外泌体的物理表征特性,一直是科研人员面临的挑战。传统光学方法受限于分辨率,难以捕捉单颗粒层面的关键数据。而基于RPS(电阻脉冲感应)原理的 NanoCoulter™纳米库尔特颗粒分析仪,以媲美电镜的单颗粒检测能力,为外泌体研究提供了更高精度、更高灵敏度且操作便捷的表征手段。
NanoCoulter™的技术实力在学术界得到了越来越多的关注,近期多篇研究工作引用并验证了其在外泌体表征方面的优势。本文将为大家盘点几篇最新的学术论文,共同探讨纳米库尔特技术如何助力科研突破,为纳米生物学研究开辟新路径!
01

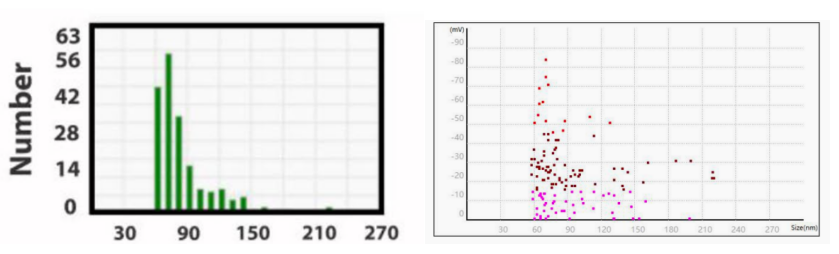
本文探讨了桔梗来源的细胞外囊泡 (PGEVs) 在三阴性乳腺癌 (TNBC) 治疗中的潜力。研究发现,PGEVs通过抑制肿瘤细胞增殖、诱导细胞凋亡、促进肿瘤相关巨噬细胞 (TAMs) 向M1表型极化,并调节肠道菌群,显著抑制了TNBC的生长。PGEVs在口服和静脉注射后均表现出良好的生物分布和生物安全性,能够有效积累在肿瘤部位,并通过增强系统性抗肿瘤免疫反应和调节肠道菌群,显著改善了TNBC的治疗效果。研究结果表明,PGEVs是一种天然的、生物相容性良好的纳米治疗候选物,适用于TNBC的治疗。
文中使用NanoCoulter™精确表征了PGEVs的粒径和Zeta电位,帮助研究者分析PGEVs的粒径分布及表面特性,证明了PGEVs具有良好的稳定性,适合作为潜在药物应用于纳米治疗。
02

研究者们深入探讨了鱼腥草来源的外泌体样纳米颗粒 (HELNs) 治疗小鼠结肠炎方面的潜力。HELNs显著减轻了葡聚糖硫酸钠 (DSS) 诱导的小鼠结肠炎,缓解了结肠炎症状及组织病理学损伤。此外,HELNs能够特异性地靶向发炎的结肠组织,调节免疫环境,并减轻炎症反应。结合NLRP3基因敲除小鼠的使用,RNA测序分析显示,HELNs抑制了NLRP3/NOD样受体信号通路。最后,HELNs还平衡了结肠炎小鼠的肠道微生物群组成,降低了有害细菌的丰度,并增加了这些小鼠肠道中有益细菌的丰度。
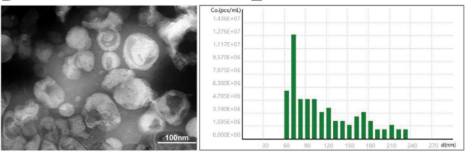
文中借助透射电镜 (TEM) 和NanoCoulter™对HELNs的粒径和浓度进行了精确测量,这些表征结果为后续的实验和机制研究提供了基础数据。
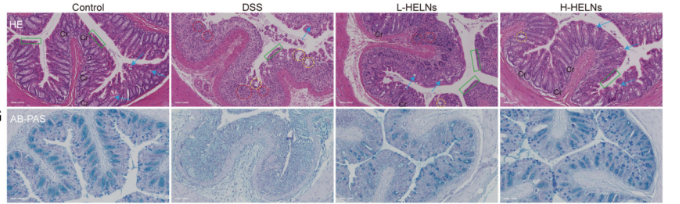
在对照组中,结肠组织组织形态正常,上皮细胞排列有序,杯状细胞充足,粘膜完整性保留,粘膜下层离散;DSS 诱导的小鼠结肠炎表现为严重的上皮萎缩,杯状细胞丢失,广泛的隐窝耗竭,固有层中明显的炎性细胞浸润和粘膜下增厚;HELNs 以剂量依赖性显著减轻了 DSS 诱导的病理损伤,可观察到的隐窝腺,局限于固有层的炎症浸润,没有明显的混合浸润,受损的上皮细胞减少和杯状细胞增加。
03

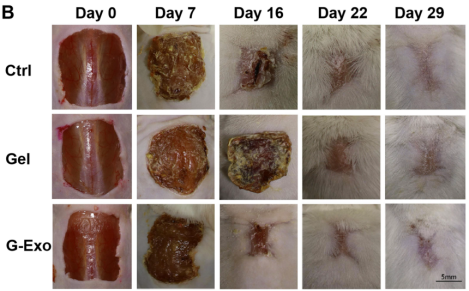
04

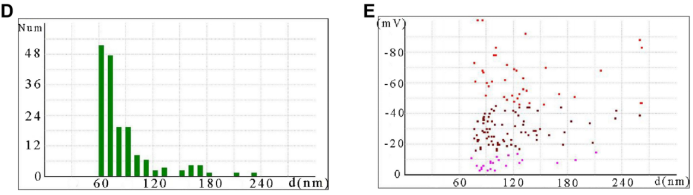
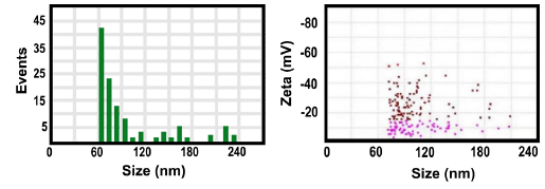
文中借助NanoCoulter™精确表征了G-Exo的粒径和Zeta电位,帮助研究人员确认G-Exo的粒径分布及表面特性,证明了G-Exo良好的稳定性,适合应用于生物医学领域。
05

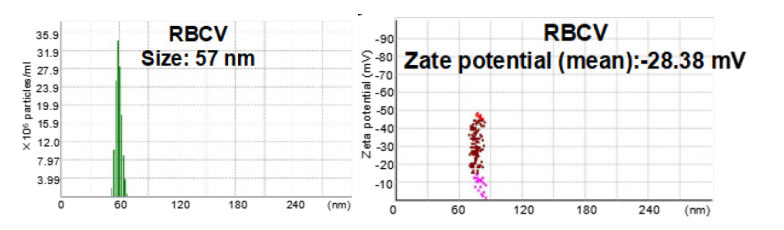
文中使用NanoCoulter™对RBCVs的粒径分布和Zeta电位进行了表征,这些数据对于评估药物递送系统的稳定性至关重要。借助RPS技术,研究人员能够优化RBCVs的制备过程,验证其理化性质,为其在治疗中的应用提供了重要的实验依据。
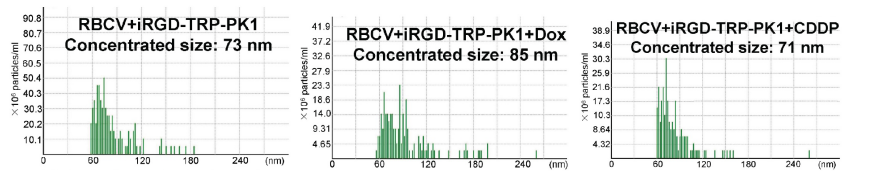
NanoCoulter™不但在细胞囊泡的应用中展现出卓越的精确度、稳定性,在材料科学中对无机纳米颗粒的表征同样发挥着不可或缺的作用 [1]。
参考文献
1.Yang M, Guo J, Li J, et al. Platycodon grandiflorum-derived extracellular vesicles suppress triple-negative breast cancer growth by reversing the immunosuppressive tumor microenvironment and modulating the gut microbiota. J Nanobiotechnology. 2025;23(1):92. Published 2025 Feb 7. doi:10.1186/s12951-025-03139-x
2.Li J, Xu J, Huang C, et al. Houttuynia cordata-Derived Exosome-Like Nanoparticles Mitigate Colitis in Mice via Inhibition of the NLRP3 Signaling Pathway and Modulation of the Gut Microbiota. Int J Nanomedicine. 2024:19 13991–14018. doi:10.2147/IJN.S493434
3.Meng D, Li Y, Chen Z, et al. Exosomes Derived from Antler Mesenchymal Stem Cells Promote Wound Healing by miR-21-5p/STAT3 Axis. Int J Nanomedicine. 2024:19 11257–11273. doi:10.2147/IJN.S481044
4.Yang S, Guo J, Chen D, et al. The Cardioprotective Effect of Ginseng Derived Exosomes via Inhibition of Oxidative Stress and Apoptosis. ACS Appl Bio Mater. Published online December 31, 2024. doi:10.1021/acsabm.4c01644
5.Bai S, Wang Z, Zhang Y, et al. iRGD-TRP-PK1-modified red blood cell membrane vesicles as a new chemotherapeutic drug delivery and targeting system in head and neck cancer. Theranostics. 2025;15(1):86-102. Published 2025 Jan 1. doi:10.7150/thno.99481
6.Pan C, Tian A, Wu M, et al. Photonic-Crystal-Printed Fabrics with Wash Resistance Properties for Color Stability Based on Hot Press Printing of ZnS Nanoparticles. ACS Appl. Nano Mater. 2024, 7, 20, 23722–23732. doi:10.1021/acsanm.4c04116
- 收藏




